올해 12월 품목허가 승인 예정, 2024년 본격 판매방교사업장 연간 200만개 혈액투석기 생산 설비 구축, GMP인증 완료국내 혈액투석기 및 소모품 수입 연간 약 1조8000억 시장 진입 초읽기
시노펙스가 8월 국내 최초 혈액투석기 관련 GMP 인증 획득 완료 후 의료기기 ‘제조업허가’를 획득했다고 25일 밝혔다.
이는 식품의약안전처로부터 의료기기 제조를 위한 입허가를 받은 것으로, 최종 ‘제조허가(품목허가)’를 받기 위한 절차에 일환으로 그 의미가 있다.
시노펙스 방교사업장은 혈액투석기 관련 글로벌 기업인 독일 알파플랜과 협력해 연간 200만개의 혈액투석기 생산이 가능한 설비를 구축했으며, 올해 8월 식품의약안전처로부터 △혈액투석기 △CRRT기기 △이동형 인공 신장기 생산을 위한 GMP(의료기기 제조 및 품질관리 기준 적합인증서) 인증을 국내 최초로 획득 한 바 있다.
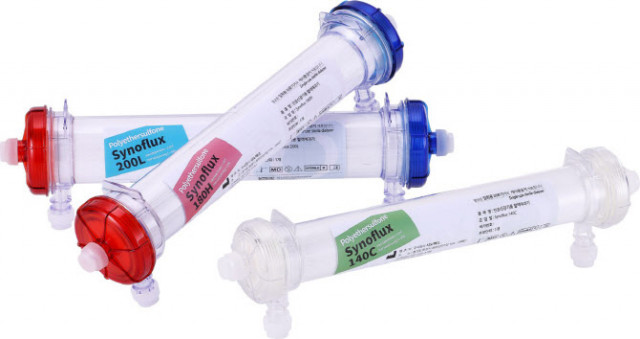
또 이미 △혈액투석기 11종 △CRRT 기기 △이동형 인공 신장기 △CRRT 혈액회로 제품을 개발, 국내·외 신장학회와 병원을 대상으로 사전 마케팅을 진행했고, ‘Synoflux’로 상표권 등록 마쳤기 때문에 품목허가 완료 즉시 본격적인 판매에는 차질이 없을 것이라고 밝히기도 했다.
올해 국내 혈액투석 관련 시장은 혈액투석기 등 소모품 분야만 1조8000억원 규모로 예상되나, 앞으로 혈액투석 필요 환자수는 더욱 급증할 것으로 전망되고 있는 상황이다.
<저작권자 ⓒ 더뉴스프라임, 무단 전재 및 재배포 금지>
박현아 기자 다른기사보기




